Brasatura in forno: componenti gassosi dell’atmosfera
Brasatura in forno: componenti gassosi dell’atmosfera
Il monossido di carbonio (CO) è un gas attivo per la riduzione di alcuni ossidi metallici (es ferro, nichel, cobalto e rame) a temperature elevate. Il monossido di carbonio però è fonte di carbonio desiderabile nell’arricchimento di alcuni acciai al carbonio ma è indesiderato nel processo di brasatura perché può rilasciare ossigeno. Il monossido di carbonio può essere generato dai residui di olio sul giunto a temperature di brasatura.
L’anidride carbonica (CO2) è neutra per la maggior parte dei metalli ed è un gas inerte di alcune atmosfere di brasatura, tranne quando si decompone in monossido di carbonio o carbonio e ossigeno, che reagiscono con i metalli.
Il metano (CH4) può provenire dal gas atmosferico generato da materiali organici lasciati sul pezzo da una pulizia inadeguata.
L’ossigeno (O2) libero nell’atmosfera di brasatura è sempre indesiderabile.
L’azoto (N2) è utilizzato in atmosfera controllata come gas di trasporto per altri gas. Un’atmosfera di azoto è applicabile ogni volta che viene utilizzato gas esotermico o ammoniaca dissociata come gas riducente. L’azoto è inerte per la maggior parte dei metalli.
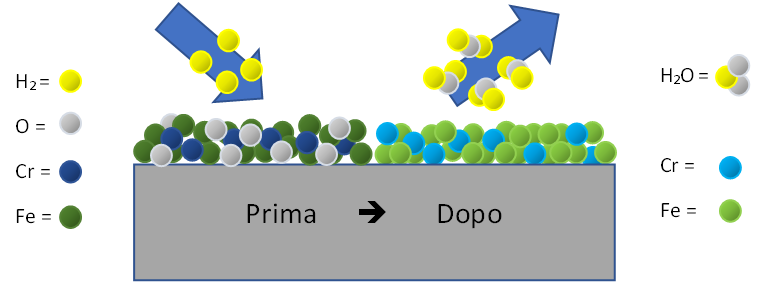
Idrogeno (H2). Le atmosfere riducenti non solo impediscono la formazione di ossidi superficiali sul metallo base alla temperatura di brasatura, ma riducono anche gli ossidi superficiali residui e gli ossidi che si formano durante le fasi a bassa temperatura del processo di riscaldamento. Sebbene alcune atmosfere riducenti possano essere utilizzate per brasare metalli i cui ossidi si riducono facilmente, atmosfere contenenti grandi quantità di idrogeno sono più adatte per la brasatura ad alta temperatura. L’idrogeno è uno dei gas più attivi per la riduzione degli ossidi per molti metalli. Se un metallo ossidato è riscaldato a una temperatura sufficientemente alta in un’atmosfera di idrogeno secca, l’ossido si ridurrà formando vapore acqueo. Il gas dell’atmosfera riducente (es. H2), in presenza di calore innesca una reazione chimica di rimozione dell’ossido metallico con la formazione di vapore:
 Ossido metallico + Idrogeno è Metallo + H2O
Ossido metallico + Idrogeno è Metallo + H2O
Vapore acqueo (H2O). È negativo in quanto la sua presenza può favorire l’ossidazione. Il vapore acqueo può essere causato da trafilamenti d’aria o d’acqua. T
Argon (Ar) ed Elio (He). Le atmosfere di gas inerte possono essere utilizzate per brasare la maggior parte dei metalli. Tuttavia, sono più utili nella brasatura dei metalli di base le cui proprietà sono influenzate negativamente dall’esposizione all’idrogeno. Ad esempio, le leghe di titanio, zirconio, niobio e tantalio sono estremamente sensibili alla presenza di minime quantità di idrogeno e si infragiliscono. Tali metalli possono essere brasati in modo soddisfacente in un’atmosfera controllata di argon o elio. Sebbene sia l’argon che l’elio possano essere utilizzati per la brasatura in atmosfera controllata, l’argon è più frequentemente utilizzato. L’argon commerciale è disponibile con una purezza garantita del 99,996%. Nel processo di brasatura in forno ad atmosfera controllata è consigliabile utilizzare Argon 4.8.
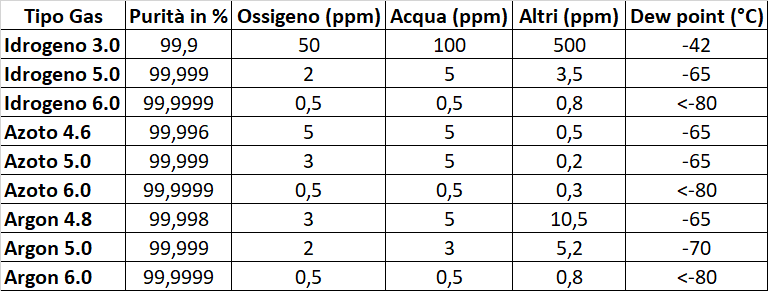 Valori di purezza di idrogeno, azoto e argon.
Valori di purezza di idrogeno, azoto e argon.
